





來源:高分子科學前沿|
發表時間:2025-05-12
點擊:3364

超螺旋結構在自然界中廣泛存在,在維持生物體系的穩定性、適應性及功能性方面發揮著重要作用。膠原蛋白作為一種關鍵的結構蛋白,由三條左手α鏈纏繞形成右手超螺旋,其分級結構與動態構象適應性共同賦予其優異的結構支撐能力,并參與多種生命過程的調控。在人工系統中構建具備類似天然體系的結構復雜性和動態可逆手性行為,依然面臨著顯著的挑戰。
近日,鄭州輕工業大學劉春森教授、荷蘭埃因霍溫理工大學E. W. Meijer教授、李晶晶博士、天津大學宋健教授等合作,以鳥苷和吡啶-4-硼酸為前驅體,利用酶催化的化學反應網絡,構筑了首例化學燃料驅動的仿生自調節水凝膠(圖1)。該體系能夠在不經過溶液相的情況下,實現自發的Gel–to–Gel轉變,并伴隨超螺旋到單螺旋的手性反轉。與傳統的Gel–Sol–Gel體系相比,該系統的獨特優勢在于具備動態穩定性,在結構轉變時維持三維網絡連續性;具備跨尺度可控性,能夠實現從分子手性到超螺旋拓撲的多級動態調控;具備仿生適應性,能夠模擬膠原蛋白的超螺旋結構與應力響應行為。目前的發現為開發可編程仿生手性軟材料提供了全新思路。該研究以題為“Self-Regulating Hydrogel with Reversible Optical Activity in Its Gel-to-Gel Transformation”的論文發表在《J. Am. Chem. Soc.》上。李晶晶博士為該論文第一作者。


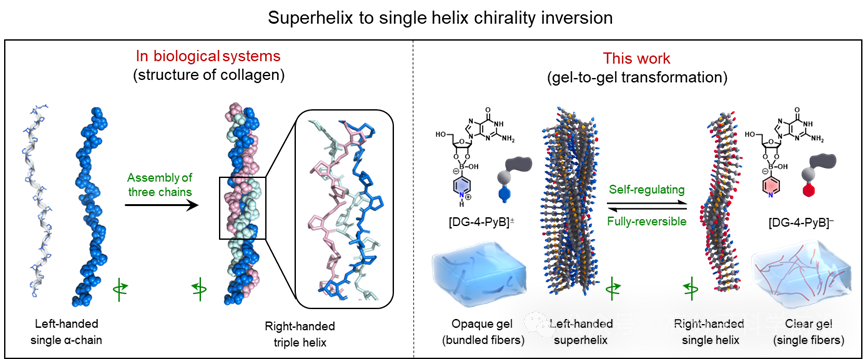
圖1|膠原蛋白與人工超分子體系中超螺旋與單螺旋結構的手性反轉。
【熱凝膠和pH依賴的超分子手性】
首先,采用常規的加熱-冷卻方法研究了天然鳥苷(D-Guanosine, DG)和吡啶-4-硼酸(4-PyB)混合物在熱力學平衡條件下的pH依賴凝膠特性和光學活性(圖2)。研究表明,G和4-PyB在pH 3.0-10.0范圍內具有廣泛的成膠能力,并且在酸性、中性和堿性條件下表現出連續的超分子手性反轉效應。組裝機理研究表明(圖3),在堿性條件下,G和4-PyB生成陰離子的硼酸酯化合物[DG-4-PyB]?,其通過氫鍵和π-π堆積相互作用,形成右手螺旋的G-四鏈體結構。Cryo-TEM顯示凝膠為單纖維結構。在酸性條件下,G和4-PyB生成兩性離子的硼酸酯化合物[DG-4-PyB]±。其自組裝形成右手螺旋的G-四鏈體結構。而中性條件下,[DG-4-PyB]±和[DG-4-PyB]?共組裝,形成左手超螺旋的纖維束結構。
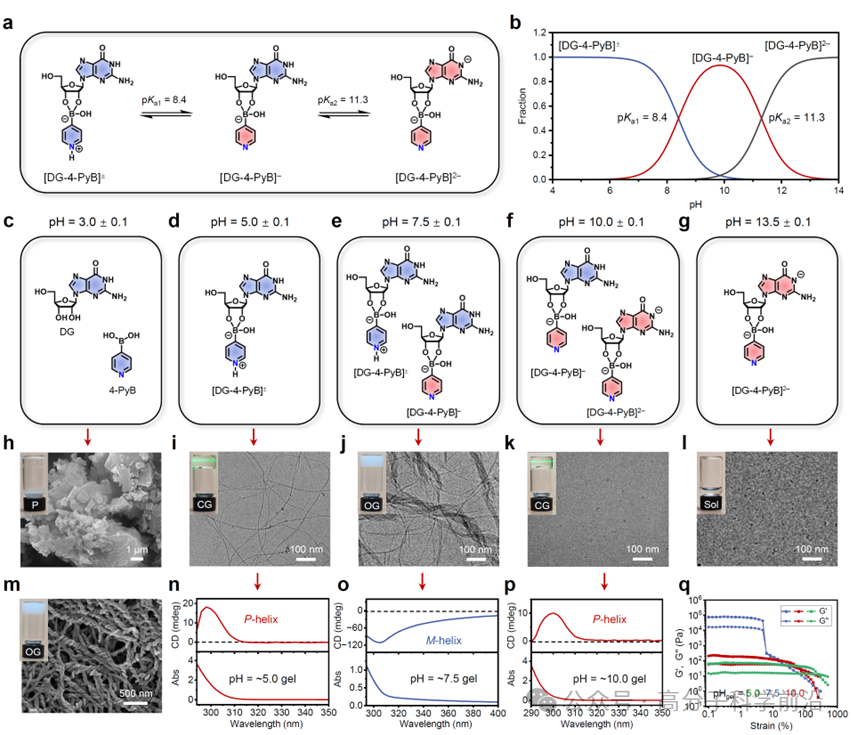
圖2|熱引發的自組裝和pH依賴的光學活性
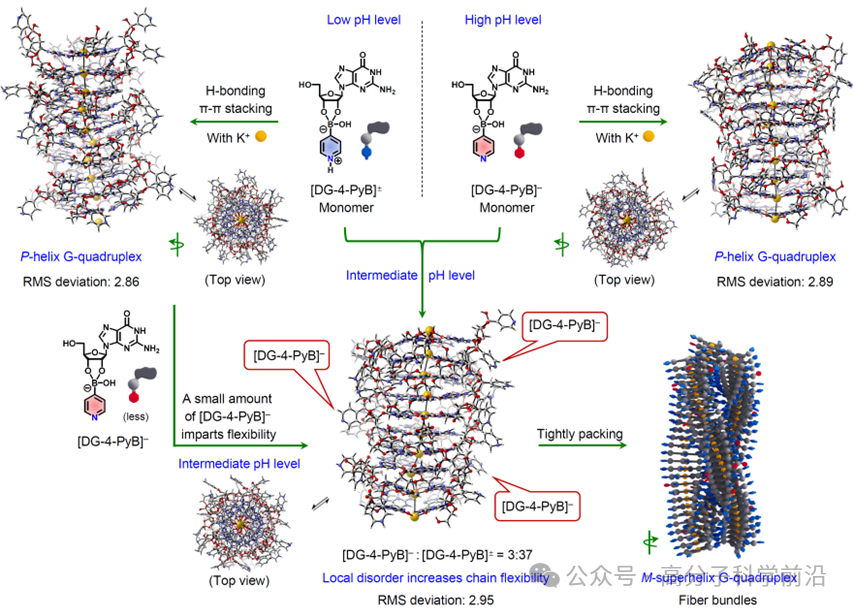
圖3| pH依賴的組裝機理
【自調節的Gel-to-Gel的轉變和超分子手性反轉】
基于課題組前期所開發的硼酸酯基的化學反應網絡(Angew. Chem. Int. Ed. 2022, 61, e202114471; Nat.Commun. 2023, 14, 5030),本研究使用脲酶和酯酶為化學燃料,構筑了一個pH-反饋體系,并詳細研究了其在pH升高-降低的連續變化過程中的凝膠情況和超分子手性變化情況(圖4)。結果表明,該體系可經歷四種不同的凝膠狀態和三種手性光學狀態(M-超螺旋、P-單螺旋及宏觀無手性態)之間的可逆轉變。凝膠在宏觀上經歷從不透明凝膠→透明凝膠→半透明凝膠→全透明凝膠”的演變,其機械性能隨pH變化和凝膠狀態變化發生自適應調節。該體系區別于傳統的Gel–Sol–Gel模式,最大的創新在于無需經歷溶膠態即可實現直接的Gel-to-Gel轉變,同時伴隨超分子手性從超螺旋向單螺旋結構的動態可逆切換,展現出優異的動態穩定性和結構調控能力。這一策略為構建具有動態調控能力和可編程手性光學性能的自調節軟材料提供了全新思路。
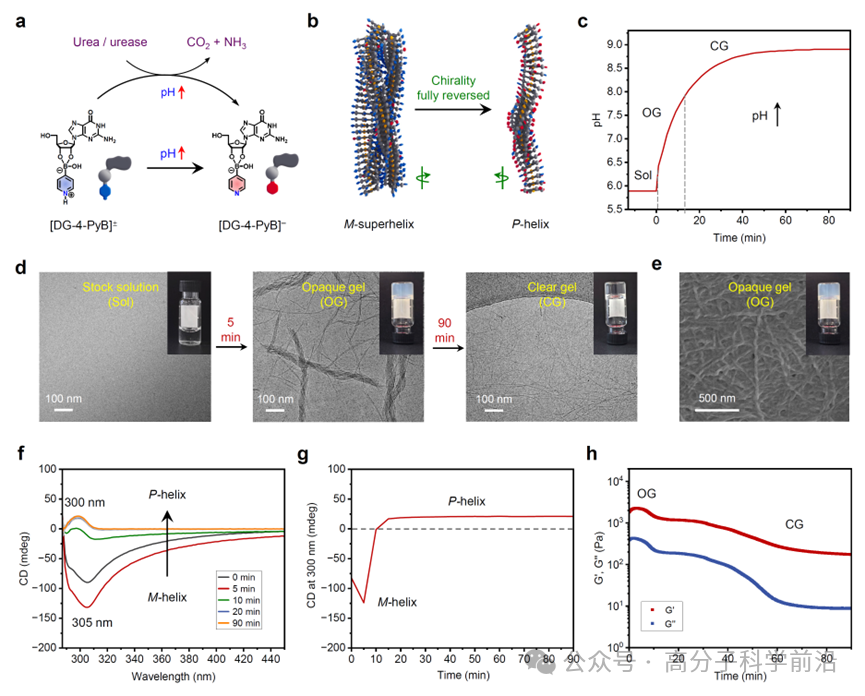
圖4|自調節的Gel-to-Gel的轉變和超分子手性反轉
【小結】
該研究構建了一種新型超分子凝膠體系,首次實現了在不經過溶液相的情況下完成凝膠-凝膠(Gel-to-Gel)直接轉變,并伴隨超螺旋與單螺旋結構間的光學手性可逆切換。該體系以中性條件下呈sp3雜化結構的4-吡啶硼酸與鳥苷為構筑單元,結合酶催化反應網絡,實現對體系pH的自主動態調控。在結構轉變過程中,凝膠保持三維網絡的連續性,展現出優異的宏觀穩定性,同時實現對手性、形貌及力學性能的精準調節。該體系集成了分級自組裝、動態手性反轉與自調節機制,為可編程仿生手性軟材料的設計提供了全新策略。
“本文由新材料在線?平臺入駐媒體號高分子科學前沿提供,觀點僅代表作者本人,不代表本網站及新材料在線?立場,本站不對文章內容真實性、準確性等負責,尤其不對文中產品有關功能性、效果等提供擔保。本站提醒讀者,文章僅供學習參考,不構成任何投資及應用建議。如需轉載,請聯系原作者。如涉及作品內容、版權和其它問題,請與我們聯系,我們將在第一時間處理!本站擁有對此聲明的最終解釋權。”

